对于国内创新药企业而言,落后并不可怕,可怕的是比你优秀的公司比你更努力。
当国内还在批量内卷GLP-1大分子的时候,海外一个全新颠覆式技术的商业化时代,正在跑步进场。
11月1日,FDA的一个独立专家小组对CRISPRTherapeutics和福泰制药共同开发的首个针对镰刀状细胞贫血病(SCD)和输血依赖性β地中海贫血(TDT)的CRISPR基因编辑疗法exa-cel做出了积极回应。
尽管外部委员会对FDA审批产品不会产生约束,但FDA将在12月8日审评这项疗法,如果如期获批,那么exa-cel将成为全球第一个获得FDA批准的基因编辑疗法。
1、不止罕见病,基因疗法正在挑战各大领域
基因治疗可以分为转基因和基因编辑两大类,简单来说,转基因疗法的原理是当我们的基因出现问题时,我们将功能正常的基因替换掉出问题的基因;基因编辑则是将出问题的基因进行修复。如果把基因组看成中央处理器,基因则是处理器上的零器件,可以理解成:转基因是替换,基因编辑是修复。
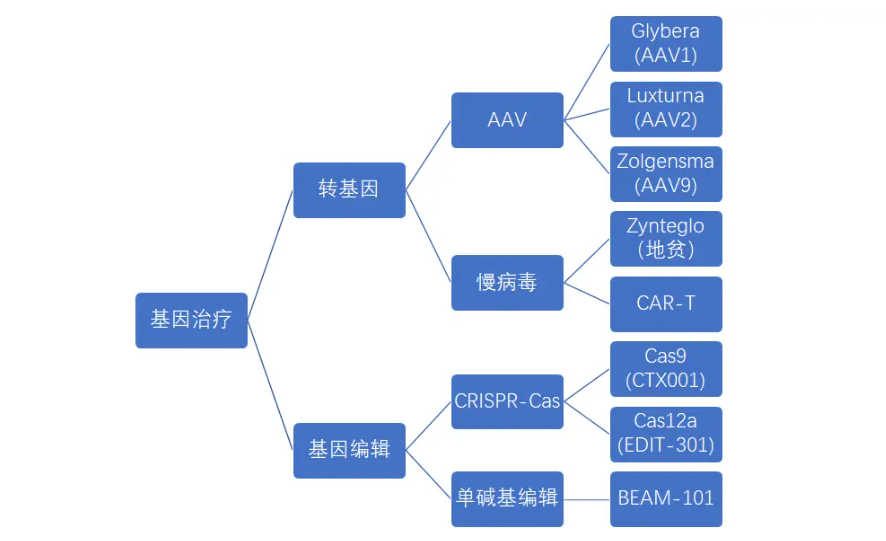
基因疗法的分类
相比转基因疗法而言,这是一种历史更短的新型基因疗法(CRISPR技术2012年出现,2020年获得诺贝尔奖),两者的核心要领转截然不同,基因技术的难点在于递送系统,载体需要将目的基因整合到细胞的基因组;而基因编辑技术则需要精确的查找替换功能,准确找到需要剪切、插入、替换的基因,以进行编辑。
目前阶段来看,基因编辑技术刚刚准备商业化阶段,而基因治疗领域更成熟的转基因疗法,已经在多个慢病领域展现出相比传统疗法的“颠覆属性”。
大分子减重药物准备冲击“药王”之时,减重基因疗法已经准备进入临床阶段。FractylHealth公司2023EASD公布数据显示:GLP-1胰腺靶向基因疗法在临床前啮齿类动物实验中第15天的总体重降低24.8%,GLP-1受体激动剂对照组降低体重18.4%。
高血压传统药物同样面临基因疗法的挑战,Alnylam的Zilebesiran是一款靶向表达血管紧张素原(AGT)的基因疗法,该药可以降低血管紧张素的水平,从而实现了24小时内持续、持久的血压控制,一针注射后疗效可持续6个月。在降血压效果方面,其公布的一期临床数据显示:第三个月时,无论高低剂量组,24小时平均收缩压降幅均超过15mmHg;如传统药物阿利沙坦当年三期数据显示,第三个月后收缩压降幅在15.3mmHg和14.9mmHg,这意味着Zilebesiran的疗效媲美传统沙坦类药物,且更加长效,提升了患者的依从性。
降血脂领域则是最先被基因疗法突破,诺华的长效降脂基因疗法Inclisiran已经在全球各地上市,其稳定控制患者血脂水平效果媲美常规PCSK9单抗,同时具备6个月注射一次的良好给药属性。Inclisiran在2021年底被FDA批准,2022年销售额1.12亿美元,2023年上半年1.42亿美元,呈现快速放量的良好趋势。
2、全球一哥礼来,近来重仓基因疗法
全球巨头药企正在频繁加码基因疗法,其中“市值一哥”礼来的动作备受市场关注。
短短的1年左右时间内,礼来已经在基因疗法领域完成了四笔重磅交易。
2022年10月,礼来斥资约6.1亿美元收购Akouos,该公司特色是拥有腺相关病毒(AAV)载体文库与创新的递送系统,以开发治疗各种感觉神经性耳聋。
2023年5月,礼来与基因编辑公司Scribe达成合作,共同开发针对特定神经和神经肌肉疾病的“体内基因编辑疗法”,交易总价超15亿美元,
2023年6月,礼来与Verve公司达成合作,重点推进Verve针对脂蛋白(a)的临床前“体内基因编辑疗法”,交易总价超5亿美元。
2023年10月,礼来与Beam达成协议,将获得Beam早前与Verve共同开发和商业化心血管疾病碱基编辑项目的选择权,交易总价将达到6亿美元。
值得注意的是,礼来经过与Beam的交易,几乎囊获了Verve公司所有的在研管线,表达出对该公司技术平台的高度认可。
Verve致力于通过碱基编辑技术开发心脏病预防针,从Beam和Acuitas分别获得碱基编辑技术、LNP递送系统的专利授权,目前公司核心管线为PCSK9靶向候选疗法VERVE-101和VERVE-102,以及ANGPTL3靶向在研疗法VERVE-201。值得注意的是,VERVE-101在10月底刚刚获得FDA临床批准,这是美国首个进入临床阶段的在患者体内进行单碱基编辑的疗法。
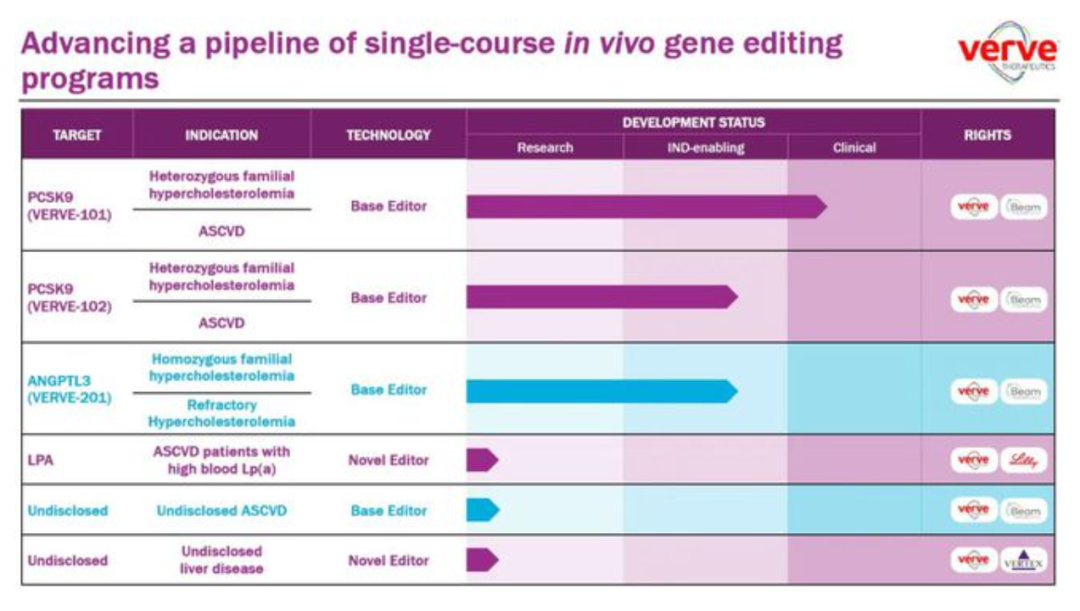
与即将有产品进入商业化的CRISPR技术相比,单碱基编辑无需切断DNA双链,就能够完成基因的精准编辑。另外,VERVE-101采用的是LNP递送(在人体内短暂存在),进一步降低了单碱基编辑的脱靶风险。这是更新一代的基因编辑技术,有望通过一次治疗便实现治愈。
3、国内进展
基因编辑作为在基因疗法中新兴的领域,尽管目前体外使用CRISPR工具改造靶细胞的做法已经得到广泛应用,但这种体外基因编辑在制备成本角度(制备成本高)和适用疾病范围(集中在单基因遗传病)仍存在较大的问题;人们把目光更多聚集在体内基因疗法领域,虽然技术难度大,但适用疾病种类丰富。
由此,国内也涌现了一批体内基因编辑的Biotech,各自均有自己独特的基因编辑系统,但大部分管线仍处于较早期的阶段;同时,我们并未在这个领域看到上市公司的身影。
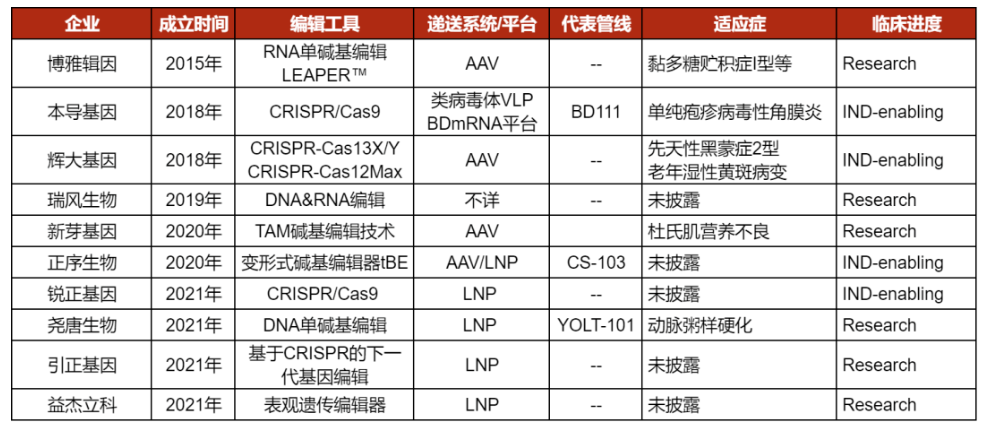
不过,在目前发展最为成熟的基因疗法小核酸药物领域,国内已经有多家企业通过自主研发、外部引进等方式进行布局,集中在肿瘤、慢病、传染病三大领域。
国内管线进度最快的无疑是瑞博生物,目前瑞博生物拥有超过4款临床阶段的小核酸药物管线,其中进度最快的为治疗2型糖尿病的SR062(二期)和治疗缺血性视神经病变的S061(三期),均从海外引进。
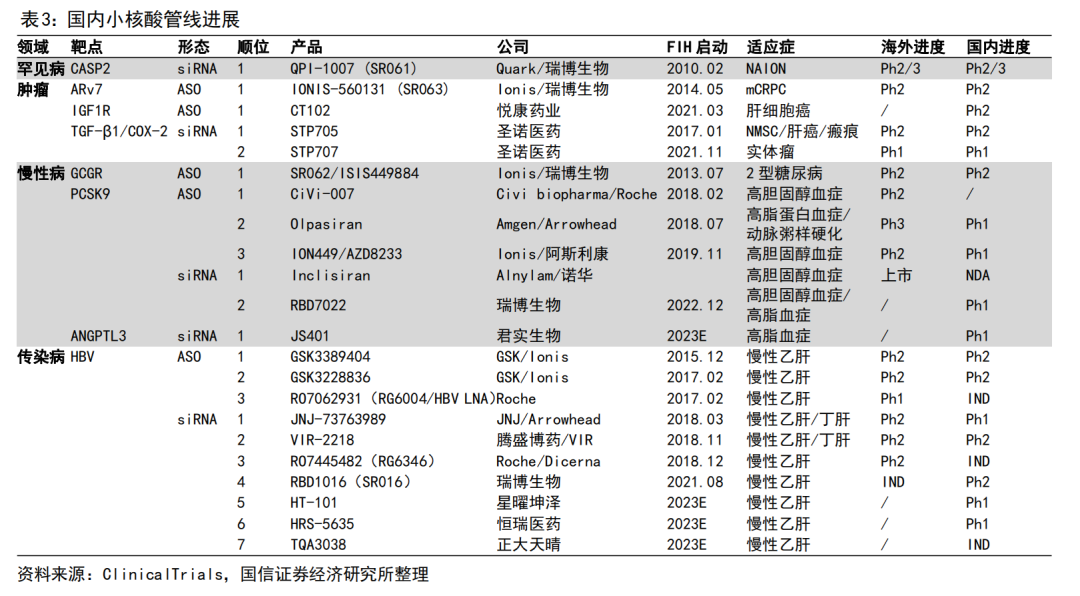
上市公司方面,君实生物首先在降血脂领域展开探索,首个进入临床管线JS401靶点为血管生成素样蛋白(ANGPTL3);恒瑞医药和正大天晴首个进入临床的小核酸管线均瞄准靶向乙型肝炎病毒(HBV),用于治疗慢性乙肝。
更让人注意的是靠中成药和化药起家的悦康药业,公司资料显示,在研小核酸管线有七项,进展管线最快是治疗原发性肝癌的反义核酸(ASO)药物CT102,其机理为以人胰岛素样生长因子1型受体(IGF1R)基因为靶标,从源头直接调控目标基因或蛋白的表达,从而达到治疗目的,已进入临床2期阶段。
此外,还有圣诺生物和腾盛博药拥有临床阶段的小核酸管线,分别用于治疗实体瘤和乙肝。
结语:国内的Biotech严重缺席基因疗法这个属于新时代的技术领域,其带来的负反馈已经显现:在降血脂药领域,信达生物PCSK9单抗正在被诺华的Inclisiran“逼到墙角”。
声明:本文仅作信息传递之目的,并不代表本平台观点。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间核实并处理。
来源:瞪羚社/Kris,仅供读者参考,著作权、版权归属原创者所有。转载此文是出于传递更多正能量信息之目的,侵权删






 首页
首页

 癌症科普
癌症科普

 癌症种类
癌症种类

 药品百科
药品百科

 肿瘤医院
肿瘤医院

 名医专家
名医专家

 免费试新药
免费试新药

 健康资讯
健康资讯

 癌症新方案
癌症新方案













