自身免疫性疾病新药,被视作继肿瘤新药之后的下一座金矿,正逐渐受到大小药厂的关注。而在繁多的细分市场中,免疫球蛋白A肾病(IgA肾病)的热度尤为凸显。
现阶段,全球IgA肾病治疗药物市场正保持快速增长,预计从2020年的5.67亿美元增至2025年的11.96亿美元,2020年至2025年复合年增长率达16.1%。
按照弗若斯特沙利文报告,到2030年,全球IgA肾病患者可达1016.52万人。考虑到当前IgA肾病干预方案仍以对症治疗为主,更有针对性的分子靶向药物,无疑将抢占这一未来可期的赛道。
一些MNC正在加速跑马圈地,例如诺华。在自有产品Iptacopan(LNP-023)的II期临床已取得积极结果并接近完成III期临床的情况下,6月,诺华仍以35亿美元的价格收购手握两款IgA肾病候选产品的Chinook。该交易令市场振奋,乃至于早年从另一家Biotech引进相关疗法的云顶新耀,股价也引来上涨。
但硬币还有另一面。近期,IgA肾病药物研发市场也受到诸多负面消息的冲击。
8月,刚获得FDA批准仅半年、作为IgA肾病领域首个非免疫抑制疗法的Sparsentan,在跟厄贝沙坦“头对头”的较量中,错过了III期研究的次要终点,开发公司Travere股价跌去45%;
10月16日,另一家明星公司Omeros披露,靶向补体系统MASP-2的单抗Narsoplimab(OMS721)治疗晚期IgA肾病的III期临床(ARTEMIS-IGAN)失败,并终止这一产品在IgA肾病适应症的开发。随后,Omeros股价下滑超过30%。

Omeros近五日股价走势
值得注意的是,IgA肾病领域的失败已经是Narsoplimab第二次受挫。作为首款靶向MASP-2的补体新药,2021年10月,Narsoplimab就曾因上市申请存在缺陷,被FDA驳回造血干细胞移植相关血栓性微血管病(HSCT-TMA)适应症的批准。
在创新药投资市场低迷、行业调整的当下,如何理解Narsoplimab这款潜在First-in-class产品开发中的波折?对于国内新药研发、投资来说,该案例又有何借鉴意义?就此,同写意采访了领诺医药创始人、CEO韩照中博士。
韩照中坦言,ARTEMIS-IGAN的结果可能会对国内同样靶向MASP-2治疗IgA肾病的药企造成负面影响,但Narsoplimab开发的经验或教训,恰恰是后来者成功的基石。毕竟,“做新药没有临床失败才是不正常的”。
“坦然接受新药临床试验的失败,思考后再出发,保持对创新开拓者的尊重,应该是医药界甚至整个社会的成熟标志。”韩照中说。
1、Narsoplimab的失败,做错了什么?
根据Omeros的新闻稿,对III期试验进行中期分析表明,Narsoplimab在主要终点没有达到显著差异。
具体来说,该研究的主要终点是,与安慰剂相比,通过24小时尿蛋白排泄量(UPE)评估的蛋白尿在36周时的减少情况。该研究的治疗人群为180名基线蛋白尿较高(24小时UPE>2克/天)的IgA肾病患者。
初步结果显示,与安慰剂相比,Narsoplimab并未取得统计学意义上的显著改善。安慰剂组的UPE降幅明显高于其他同类临床试验中报告所显示的安慰剂效果。
由于之前与FDA达成的协议,Omeros不会提交Narsoplimab在该适应症方面的批准申请,并将终止ARTEMIS-IGAN临床试验。
这次研究为什么失败了?等待Omeros做进一步分析、临床数据公布之前,韩照中结合从靶点、药物到临床设计的多个维度,分析其中可能的原因,以及该案例对新药研发的参照意义。
Narsoplimab的靶点选择了MASP-2——甘露聚糖结合凝集素相关丝氨酸蛋白酶-2——这是一种补体系统的凝集素信号通路的效应酶,介导了多种细胞损伤相关炎性疾病的发展进程,也包括IgA肾病。
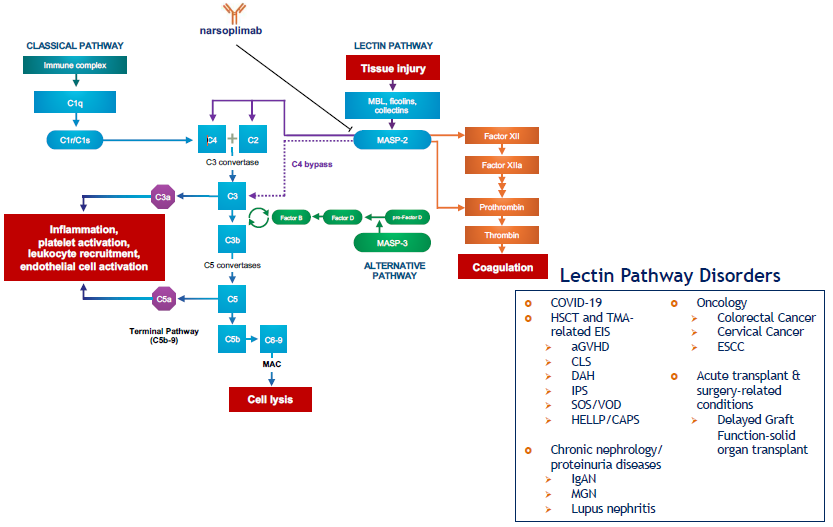
MASP-2靶点上下游通路
然而,作为创新药物靶点,MASP-2是否是疾病发生、发展的主要或唯一驱动因素?其靶向治疗对所有对应适应症人群有效,还是仅仅对部分特定人群有效?
反过来说,考虑到IgA肾病病理机制的复杂性,仅在凝集素路径介导的感染或细胞损伤相关病理过程中发挥主要作用的MASP-2,是不是IgA肾病的最好治疗靶点?在相关临床试验中,是否需要筛选MASP-2介导的凝集素路径调控、活化异常的病人入组?
此类问题都需要临床前和临床数据的支持,也有必要对临床数据做进一步的分析,以便合理判断MASP-2是否可以作为有效的疾病治疗靶点。
换言之,Narsoplimab的IgA肾病临床失败,提示靶点、适应症、或药物效应相关的生物标志物的重要性。以合理的生物标志物为导向的入组病人筛选、疗效评估,是新靶点开发的关键。哪怕是目前肿瘤免疫治疗的基石PD-1抑制剂,在总体人群中也只有20%左右的响应率。
其次,Narsoplimab的“此次”临床试验失败也不能直接跟它的“未来”画上等号。
“这个药物启动了多个适应症的临床开发,说明Omeros对这个分子是基本满意的。”韩照中提醒,Omeros宣布终止Narsoplimab针对IgA肾病的临床开发的新闻稿中,也提到近期的重点工作之一,是关注这款药物治疗HSCT-TMA的BLA申请。
至于临床设计上,除入组患者的选择应该更多关注适应人群外,韩照中还提到ARTEMIS-IGAN中对照药物的选择。
众所周知,糖皮质激素治疗IgA肾病的疗效有争议,包括该类药物的长期使用可能带来严重的毒副反应。然而,相较于无药可用,糖皮质激素在临床中仍是不少医生的首选。
Omeros发表的II期临床结果表明,Narsoplimab单药治疗在18周蛋白尿降低效果不明显,但36周至52周观察期内效果显著,尽管也观察到较大的个体差异;与激素的联合治疗中,在治疗早期(18周)即能显示显著的蛋白尿降低。
而ARTEMIS-IGAN研究中,Omeros提到对照组的蛋白尿降低水平高于预期,和未经治疗的情况下IgA肾病患者的蛋白尿水平一般会持续上升的常识不一致。“背后的原因是什么?从公开的数据资料,看不出入组病人是否接受激素的基础治疗。”韩照中表达了自己的困惑。
随着此次受挫,原本用于IgA肾病商业化和继续推进ARTEMIS-IgAN试验的资金,将被转用于Omeros的其他后期项目,包括IgA肾病旁路途径抑制剂OMS906正在进行的II期和即将进行的III期项目。或许正是基于Narsoplimab临床试验中获得经验与教训,Omeros坚定了推进补体靶向药物治疗IgA肾病的决心,只是转向补体的旁路路径为药物靶点。
2、机制与靶点:IgA肾病的“无知之幕”
约翰·罗尔斯在《正义论》中,提出一个著名的概念“无知之幕”。他设想,只有公众在被一块幕布遮住,对自己的情况不了解时,才最有可能讨论出拉开幕布后实现社会公正安排的方案。套用这个形象,科学家们面临的,则是对IgA肾病认识的难题。
跟大多数自身免疫性疾病类似,IgA肾病的发病机制并不单一、清楚。
业界比较公认的“四重打击”学说,是这样描述IgA肾病的:关键起始因素是Gd-lgA1分子的产生(第一重打击),进而识别Gd-lgA1的lgG或lgA自身免疫抗体产生(第二重打击),随着循环免疫复合物的不断形成(第三重打击),免疫复合物最终沉积膜区,诱发免疫反应,引起肾小球损伤(第四重打击)。
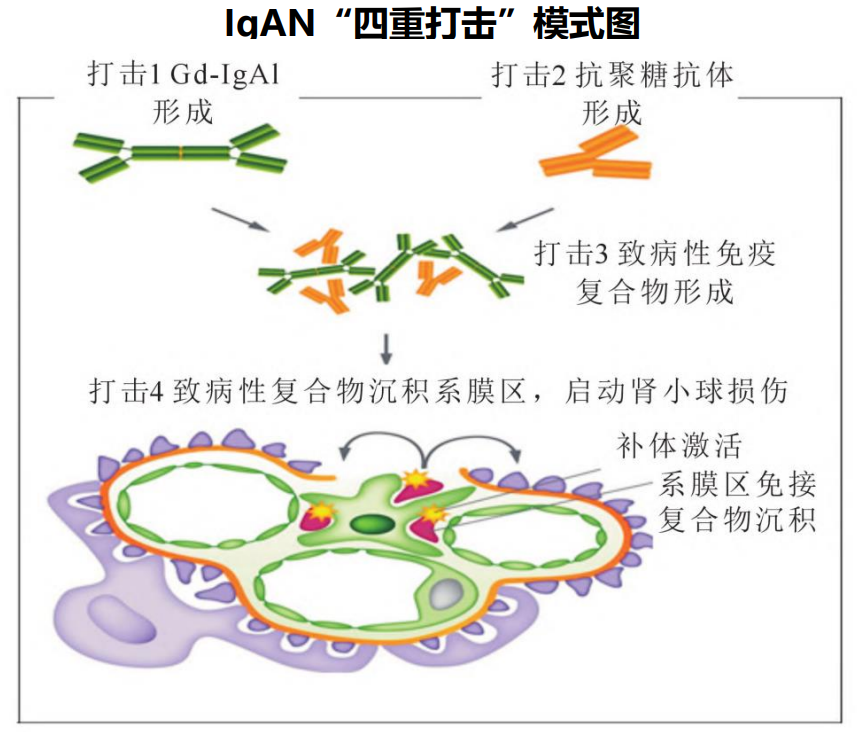
IgA肾病“四重打击”模式
但也有业内人士认为,IgA肾病并不完全具备自身免疫性疾病的特征,部分临床试验表明,免疫抑制治疗无效,因此IgA肾病更可能是炎症性疾病。
简言之,如果不能说IgA肾病疗法的开发是完全的黑箱,那么至少这个过程还有诸多尚待掀开的帘幕。
韩照中介绍,从研发策略看,除去Omeros重仓的抑制补体通路,IgA肾病靶向治疗大体还包括系统/局部免疫抑制剂、调节B细胞活化、调节非免疫通路等路径。
6月12日,诺华宣布以高达35亿美元的价格收购Chinook,就牵涉两款不同机制的IgA肾病新药。
Chinook旗下进展较快的Atrasentan,属于一种口服ETA受体的选择性拮抗剂,拟用于治疗IgA肾病和蛋白尿性肾小球疾病。目前,Atrasentan正在进行临床III期ALIGN研究,主要终点是蛋白尿的变化。
另一款Zigakibart(BION-1301)是一种APRIL单抗。APRIL在IgA肾病患者群体中升高,并与不良预后相关,Zigakibart旨在阻断APRIL与BCMA和TACI受体的结合。该药正在进行临床I/II期研究,预计将在今年进入后期研究。
耐人寻味的是,收购Chinook之前,诺华的Iptacopan的III期试验中期结果即将揭盲,诺华的“重金求药”是对靶向补体策略的担忧,抑或是一种商业策略?
韩照中的判断是后者。10月10日,根据诺华披露的最新数据,补体旁路途径靶向的LNP023在IgA肾病的临床治疗中效果显著。诺华已决定,向FDA提交加速新药上市的申请。
Iptacopan可通过抑制B因子,阻断旁路途径调控的补体活化和信号放大过程,显著减少补体异常活化造成的细胞与组织损伤,降低IgA肾病相关的蛋白尿水平。监管方面,EMA已授予Iptacopan治疗IgA肾病的孤儿药资格认定。
“现在看,旁路途径可能会是更有潜力的方向。”韩照中进一步说,“除了诺华,其他大药企比如阿斯利康也有相关在研产品,我们领诺医药的在研产品也即将进入临床。”
Omeros的转向——资金投入到IgA肾病旁路途径抑制剂OMS906——某种程度可以理解为是对这番判断的支持。
3、FICorFollow?智者的选择
2021年,补体药物领域的开拓者Alexion被阿斯利康以390亿美元收购,创下当年度国际医药市场最大商业并购记录。
如果临床试验和后续商业化成功,Omeros本可以如Alexion那样,讲述完美、励志的故事:从零起步的Biotech,深耕十余载,终于将一个全新的药物靶点成功验证,推出一款革命性的的产品服务于医疗市场,解决迫切的患者需求。可随着ARTEMIS-IGAN研究的失败,一再受挫的Narsoplimab上市之路更显遥遥无期。
Narsoplimab在IgA肾病方面探索的刹车,大概也令同样跟进MASP-2这一靶点的本土药企承受压力。
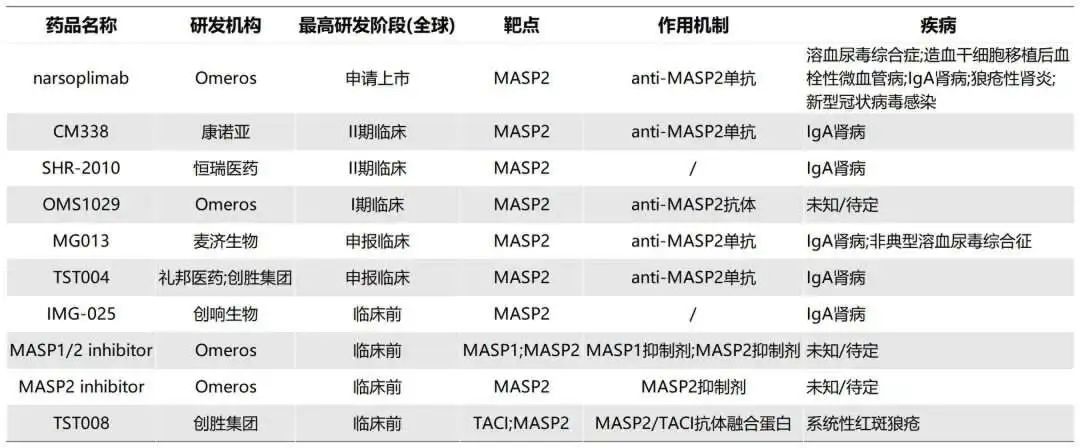
部分IgA肾病在研管线
“这个时候,你就需要说服投资人,或者更重要的是说服自己,为什么还要坚持这个靶点,”韩照中进一步回应道,“冲击和挑战还是巨大的,但有些问题并非无解。”
在他看来,此次临床试验的失败,并不是MASP-2靶点的失败,也非补体靶向策略的失败,更不是IgA肾病靶向药物的失败。相反,Narsoplimab的经验或者教训,恰恰是业界药物开发、科学研究不断进步的阶梯。
“我们可以针对性地调整靶点选择、药物设计、临床开发方案,比如用一些生物标志物,更精准地筛选病人,或更有效地评估药物的安全性和有效性。”韩照中总结说,循着别人走过的路,可以避免别人踩过的坑。
康诺亚的CM338是国内首个进入临床阶段的MASP-2单抗,根据该公司披露,CM338活性是Narsoplimab的10-50倍,并对肾组织C3、C4、IgA沉积有良好的抑制作用。恒瑞医药、创胜集团、麦济生物等药企的同类靶点竞品,也已处于临床在研阶段。
资本市场对药物研发中First-in-class、Fast-follow甚至Me-too模式的充满争论,韩照中认为,模式各有优劣,不能一棍子打死。但客观来说,随着国内外监管政策的不断调整和市场壁垒的不断消除,Fast-follow或Me-too的机会和相应的挪腾空间会越来越小。
“如果一款被跟随的First-in-class产品成功了,那么先机就被别人占据;如果它失败了,跟随者肯定也会受到负面消息的波及。”韩照中评论道。跳出Fast-follow尴尬处境的关键,离不开科学合理性、技术优越性、商业可行性的客观、准确判断,这又涉及对相关信息的收集、整理、消化、理解和相关策略的制定,等等。
总结来说,Fast-follow不是简单跟进,它意味着一套合理的研发计划,设置好每个合理的里程碑节点、客观评价指标。只有在合乎科学判断的基础上,跟踪者才有可能胜出,继而去超越First-in-class,成为Best-in-class。
回到Omeros的例子,韩照中强调,“第一个吃螃蟹”肯定会有风险,对于首创新药的开发而言,临床试验做一个成功一个,那才叫不正常。决策层面,Omeros基于临床结果快速选择退出,壮士断腕寻找一个更确定的市场,也是值得国内企业学习的地方。
谈及未来,韩照中仍对IgA肾病领域的新药抱有期待。他借用抗体药物和ADC的故事说,这些概念早在上个世纪70年代就被提出,在探索的过程中经历了各种挑战,比如安全性、有效性、可生产性甚至药物经济学等的疑问或困难,不过随着技术的迭代,关键问题得到解决,整个市场最终迎来快速增长。
“随着越来越多新靶点、新技术的探索,IgA肾病缺乏有效治疗手段的局面近几年有望得到显著转变,特别是补体靶向的药物研发目前看来,仍是最有希望的方向之一。”韩照中展望说。
Narsoplimab此次临床失败,对Omeros当然是巨大的损失,但正如韩照中的评价,对整个行业则是有很大的积极意义。“理性的失败者永远值得尊重。”
本图文来源于【药智网】仅供读者参考,著作权、版权归属原创者所有。转载此文是出于传递更多正能量信息之目的,侵权删






 首页
首页

 癌症科普
癌症科普

 癌症种类
癌症种类

 药品百科
药品百科

 肿瘤医院
肿瘤医院

 名医专家
名医专家

 免费试新药
免费试新药

 健康资讯
健康资讯

 癌症新方案
癌症新方案













