近日,亘喜生物在第65届美国血液学会(ASH)年会上以口头报告方式汇报了BCMA/CD19FasTCAR-T疗法GC012F一线治疗高危多发性骨髓瘤新确诊患者(NDMM)的一期IIT最新数据。
GC012F一线治疗NDMM临床数据惊艳
NDMM是亘喜生物基于GC012F的安全性优势,在多发性骨髓瘤领域前瞻性布局的一条赛道。早在去年ASH年会,公司就首次公布了这项IIT研究的临床数据,安全性和疗效良好;今年9月的IMS年会上又做过数据更新,此次能继续入选ASH2023口头报告,不难看出业界对于GC012F针对NDMM一线治疗抱以厚望。
截至2023年10月1日,22例可评估患者中位随访时间18.8个月,疗效方面:ORR依旧高达100%,sCR率也高达95.5%,MRD-率同样保持了100%,中位DOR和中位PFS数据尚未成熟。

图片来源:ASH官网摘要信息
安全性方面,GC012F仅27%(6/22)的患者出现细胞因子释放综合征(CRS),且均为低级别,包括1级(23%,5/22)和2级(5%,1/22)。未观察到患者出现任何级别的ICANS或其他神经毒性。
难治性系统性红斑狼疮IND获FDA批准
两周前,亘喜宣布GC012F治疗难治性系统性红斑狼疮的1/2期临床试验申请获得FDA批准。
不同于肿瘤的治疗,自身免疫性病作为一种慢性、不会迅速危及生命的疾病,监管机构对于其治疗的安全性要求更高。
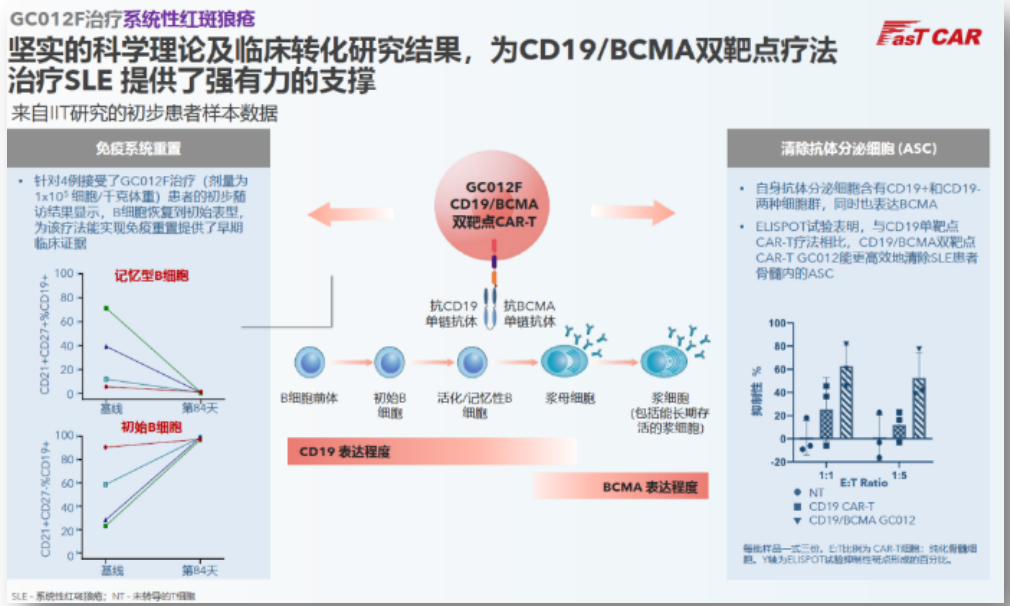
亘喜在今年5月宣布启动GC012F治疗rSLE的IIT研究,正式将双靶点CAR-T疗法拓展到自免领域。随着越来越多细胞疗法玩家加入到自免赛道的竞逐中,上个月,首届美国自身免疫性疾病细胞疗法峰会正式召开,亘喜生物CBO在会上介绍了GC012F如何应用于rSLE适应症的原理,同步披露了4例患者的早期转化样本结果:治疗后B细胞表型恢复到初始表型,初步证明了该疗法能有效实现免疫重置。
亘喜此前披露的另一项ELISPOT试验意在证明:与CD19单靶点CAR-T疗法相比,GC012F的CD19/BCMA双靶点设计,能更高效地清除产生自身抗体的B细胞和浆细胞。预计到2024年,我们可以看到更多相关数据。
图片来源:亘喜生物
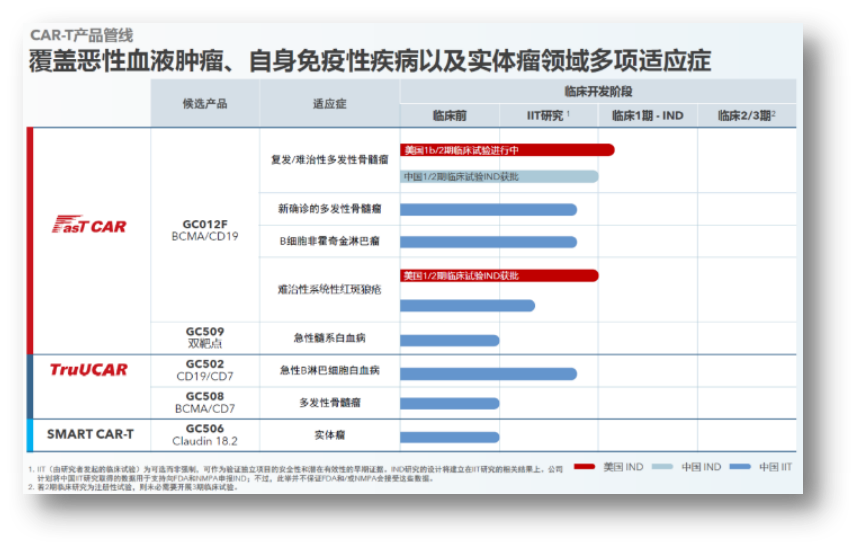
亘喜生物研发管线分析
血液瘤、实体瘤;双靶点、通用CAR-T多维度创新
除GC012F之外,亘喜生物研发管线的创新产品还包括针对实体瘤的Claudin18.2CAR-T,以及CD19/CD7CAR-T、BCMA/CD7CAR-T两款通用CAR-T疗法。
图片来源:亘喜生物
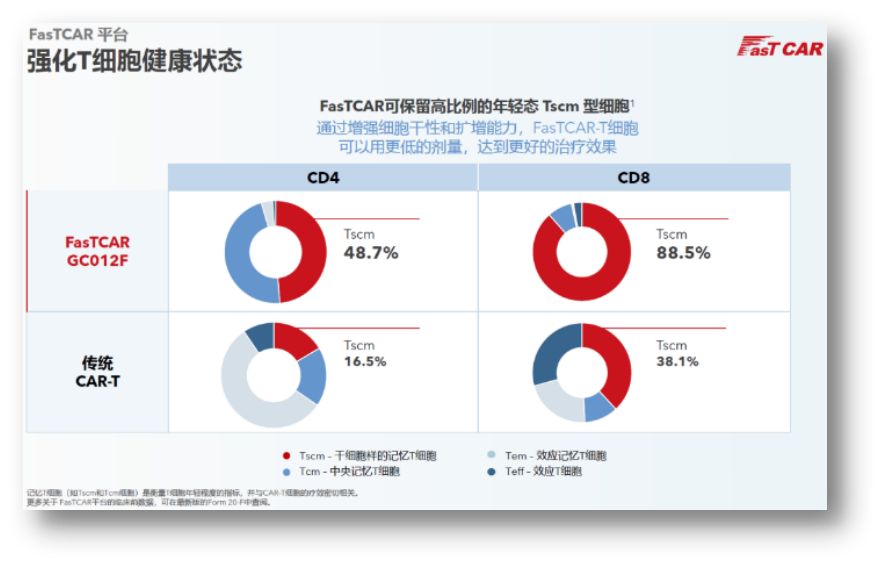
FasTCAR:高Tscm比例保留
传统CAR-T在血液瘤方面已取得诸多突破,但疗效仍有提升空间,安全性更需持续改善,工艺复杂和高成本则限制了其可及性。
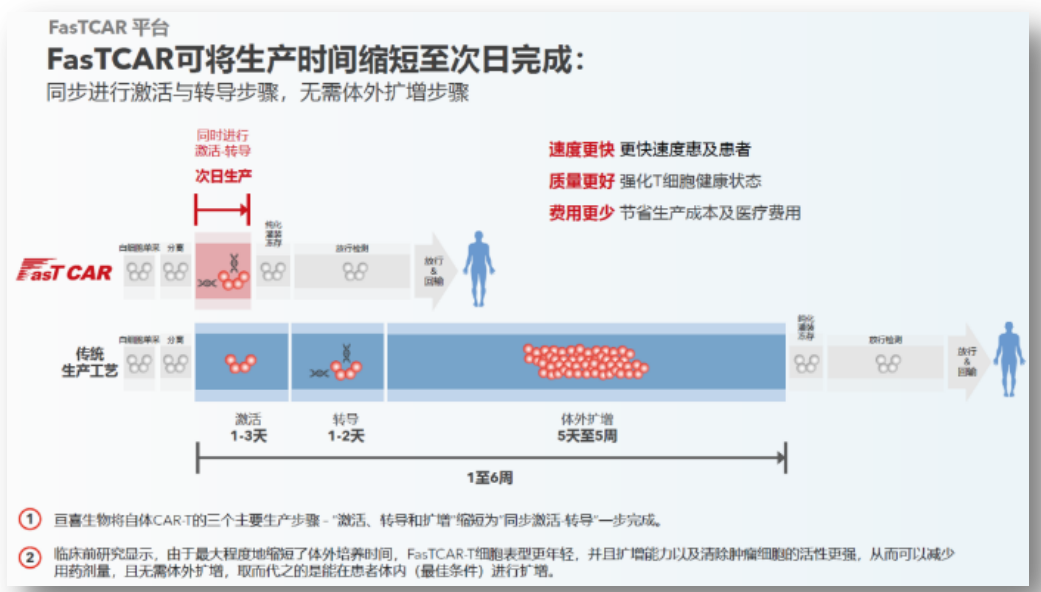
据亘喜生物消息,其建立的FasTCAR技术平台将传统CAR-T的生产时间从几周缩短到次日完成,显著降低人员及设备工时的成本。
图片来源:亘喜生物
据悉,FasTCAR保留了高比例的年轻态Tscm细胞,细胞干性的增强显著改善了CAR-T的持久性,同时可以用更低的剂量达到更好的治疗效果。GC012F正是基于FasTCAR技术平台开发的产品。
图片来源:亘喜生物
SMART CART:有望攻克实体瘤的创新技术
实体瘤一直是CAR-T疗法的难点,针对这一难题,亘喜生物开发了SMARTCART增强型技术,作为“逻辑门开关”思路的一种方案。据亘喜生物介绍,这将抑制性分子信号转化为T细胞激活信号,从而更好且更久地对抗肿瘤微环境的免疫抑制性。
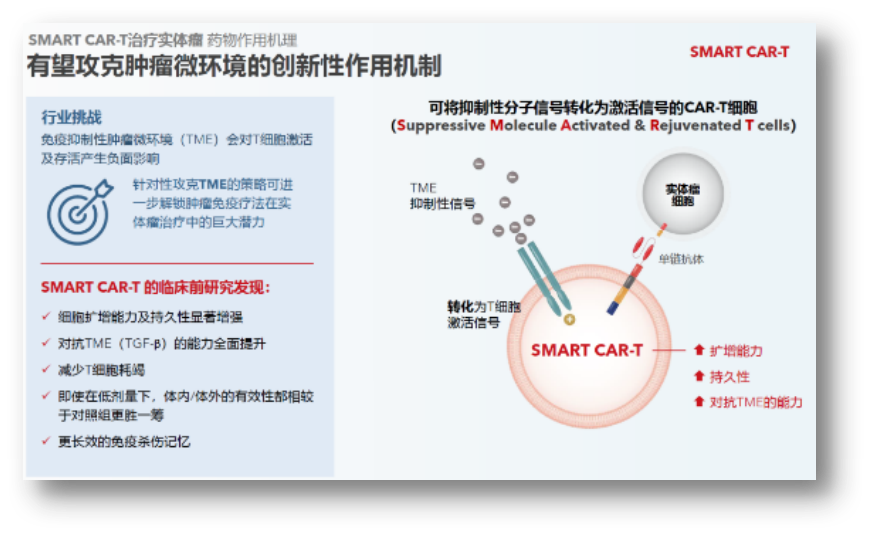
图片来源:亘喜生物
亘喜在第38届SITC年会上首次公布了SMARTCART管线产品GC506的临床前数据:对于由TGF-β介导的凋亡和耗竭的抵抗能力显著增强。在肿瘤细胞连续刺激模型中,即使面对TGF-β的抑制,SMARTCART细胞相较于传统CAR-T细胞,在体外和体内都实现了更强劲且持久的特异性肿瘤细胞杀伤。
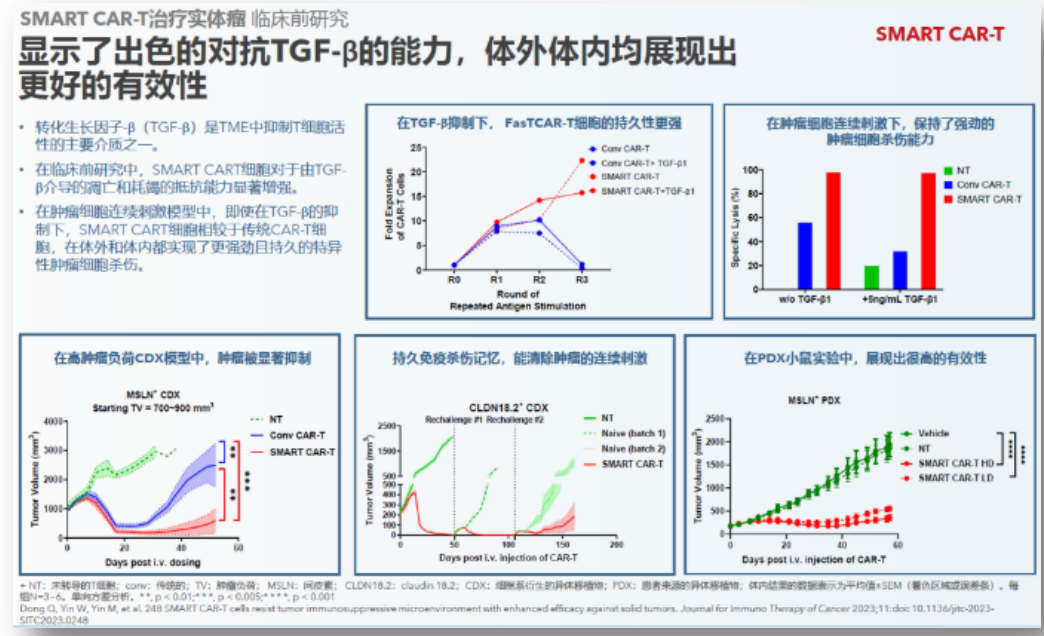
图片来源:亘喜生物
据悉,在小鼠模型中,与传统CAR-T细胞相比,SMARTCART在肿瘤连续刺激实验以及高肿瘤负荷研究中,均显示出更优的肿瘤杀伤活性。小鼠模型注射后100天以上仍保持高度有效性,注射5个月后骨髓和脾脏的CAR-T细胞仍能杀伤肿瘤细胞,经刺激后仍可以再次扩增。

图片来源:SITC官网摘要信息
TruUCAR:通用CAR-T
虽然自体CAR-T在血液瘤领域已经取得了很多突破性进展,但高成本,以及无法及时给药仍然很大程度上限制了临床上的广泛应用。因此,通用CAR-T是整个领域长久以来努力探索的重要方向。据悉,亘喜生物建立了TruUCAR技术平台,通过多种设计来避免免疫排斥,并提高持久性。具体而言,通过表达CD7CAR来靶向T细胞和NK细胞,避免HvG;通过T-AgKO防止自相残杀,通过敲除TCR避免攻击正常细胞引发GvHD等。
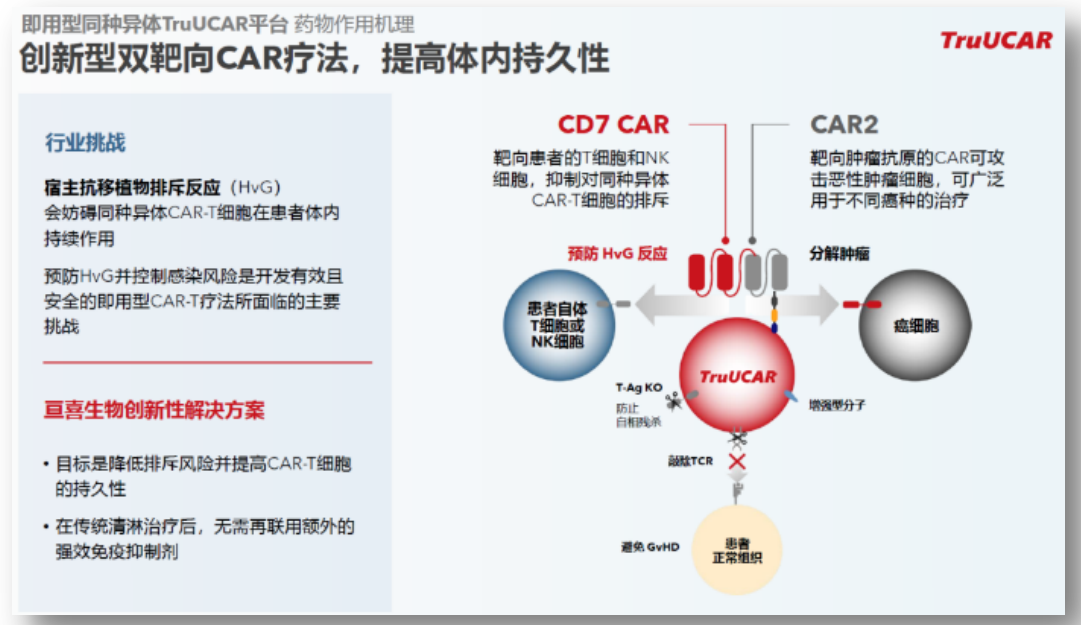
图片来源:亘喜生物
目前,GC502是基于TruUCAR技术平台开发的代表性产品,同时靶向CD19/CD7,初步临床研究表明在传统清淋后无需使用强效免疫抑制剂,目前4例患者治疗后3例达到MRD-CR/CRi,安全性方面同样具有“亘喜基因”:无4/5级CRS,无ICANS,无GvHD。初步表明TruUCAR的设计具有可行性,同时达到较理想的有效性与安全性。
结语
今年年中,VivoCapital领衔一众知名医疗行业投资者通过私募配售的方式继续“加码”1.5亿美元。由此,亘喜生物不但得到了市场与业界的进一步看好,也让资金储备更加宽裕:根据财报显示,截至三季度末账上现金为2.34亿美元,将保障公司的研发与运营到2026年下半年。期待亘喜能继续专注于推进多条亮眼临床管线的后续开发。
本文部分图文来自药智网。仅供读者参考,著作权、版权归属原创者所有。转载此文是出于传递更多正能量信息之目的,侵权删






 首页
首页

 癌症科普
癌症科普

 癌症种类
癌症种类

 药品百科
药品百科

 肿瘤医院
肿瘤医院

 名医专家
名医专家

 免费试新药
免费试新药

 健康资讯
健康资讯

 癌症新方案
癌症新方案













