病例摘要:
初始治疗
患者男性,68岁,因“大便习惯改变1月余”于2019年9月至我院就诊。查体:浅表淋巴结阴性,心肺腹部检查阴性,肛查:入肛7cm未及直肠肿物,指套无血染。家族史:哥哥肝癌病史。
辅助检查:
超声肠镜:距肛门约18-20cm直肠近端环周隆起型肿物,内镜可勉强通过,诊断:直肠癌UT4aN2。活检病理:中分化腺癌。盆腔MR:直肠肿物下缘距肛缘约13cm,长约9.2cm,累及3/4周径;肿瘤在腹膜反折上方;考虑为T4a,累及腹膜反折;肛管未受累;直肠系膜内淋巴结,考虑转移;MRF(-);EMVI(+)。全腹CT:左髂总血管旁、下腔静脉旁淋巴结,转移待排。

术前超声肠镜(2019-09)
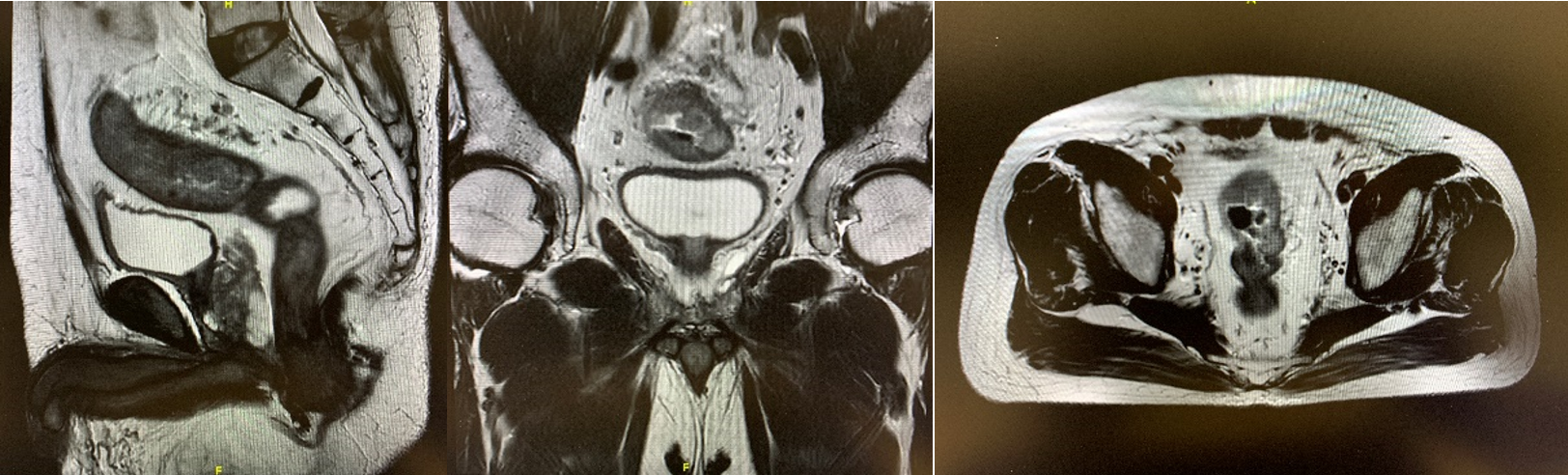
术前MR(2019-09)
入院诊断:
直肠癌cT4aN2M1
2019-10-09行腹腔镜下DIXON+腹主动脉旁淋巴结清扫术
术后病理:
(直肠)中至低分化腺癌,穿透固有肌层达结直肠旁组织(pT3),脉管内癌栓:+,神经束侵犯:+,切缘:-。淋巴结情况:(中央淋巴结)4枚,未见癌;(肠旁淋巴结)15枚,12/15见腺癌转移;(中间淋巴结)5枚,3/5见腺癌转移、(腹主动脉旁淋巴结)8枚,2/8见腺癌转移。淋巴结外肿瘤种植结节:5枚。免疫组化:pMMR,BRAF-V600E(-),HER2(0),Ki67(80%+)
基因检测:
MSS,TMB-L(9.6Muts/Mb);KRAS突变,PIK3CA突变
术后诊断:直肠癌pT4aN2bM1a IVA期,MSS
术后治疗:
术后建议行辅助化疗,2019-11-06予XELOX方案化疗1程后患者因个人原因拒绝继续接受辅助治疗。
2020-06-27复查CT:左肺尖及下叶后基底段结节,考虑转移瘤可能性大,较前新增,左下气管旁及左肺门淋巴结,考虑转移,较前新增;2020-07-01 PET-CT:左肺门及纵隔淋巴结代谢活跃,左肺尖及下叶后基底段数个结节代谢活跃,考虑转移。

复查PET-CT(2020-07)
转移后治疗:
建议患者常规化疗+靶向治疗,患者拒绝常规化疗。考虑患者TMB接近10Muts/Mb(9.6),转移灶主要局限于双肺,参考REGNOVO模式给予PD-1抗体+TKI治疗。
分别于2020-07-07、07-28、08-18、09-08、09-28、10-20予帕博丽珠单抗200mg治疗6个疗程,并予呋喹替尼3mg qd治疗。期间因腹泻、头痛等副反应改予瑞戈非尼120mg qd治疗,后仍反复出现头痛,于2020-10停用所有治疗。
2020-09-01复查CT:左肺尖及下叶后基底段结节,考虑转移瘤可能性大,较前稍缩小;左下气管旁及左肺门淋巴结,考虑转移,较前缩小;
2020-11-05复查CT:左肺尖及下叶后基底段结节,考虑转移瘤可能性大,较前稍缩小;左下气管旁及左肺门淋巴结,考虑转移,较前缩小;右侧肾上腺结节状增粗,较前新增,不排除转移可能。
2020-12-16复查CT:左肺尖及下叶后基底段结节同前,可疑转移;左下气管旁及左肺门淋巴结,可疑转移,大致同前;右侧肾上腺肿物,考虑转移瘤可能性大,较前增大。

治疗后复查(2020-12)
考虑肾上腺病灶停止治疗后出现,患者仍拒绝全身化疗,同时也无法耐受呋喹替尼或瑞戈非尼,遂决定重新引入PD-1抗体。
后于2020-12-24、2021-01-13、2021-02-02予帕博丽珠单抗200mg治疗3个疗程。
2021-02-19复查CT:左肺尖及下叶后基底段结节,可疑转移,左肺尖结节较前稍缩小,余大致同前;左下气管旁及左肺门淋巴结,稍缩小,可疑转移;右侧肾上腺肿物,考虑转移瘤可能性大,较前增大。

治疗后复查(2021-02)
肾上腺转移灶治疗:
肺部病灶控制佳,但右肾上腺结节较前增大,考虑为局限性进展;于2021-03-05行腹腔镜下右肾上腺肿物切除术,术后病理:(右肾上腺及肿瘤)中-低分化腺癌,符合肠腺癌转移,免疫组化:HER2-G(0),CK20(+),CDX2(+),SATB2(-),Melan-A(-),CgA(-),SF-1(少量+),Ki67(90%+)。
后续治疗:
考虑除肾上腺外其他病灶控制良好,建议继续免疫治疗,如能接受化疗可在PD-1抗体的基础上联合化疗。患者仍然拒绝化疗,遂分别于2021-03-29、2021-04-19、2021-05-10、2021-05-31继续予帕博丽珠单抗200mg免疫治疗4个疗程。
2021-05-17复查CT:左肺尖及下叶后基底段结节,考虑转移,其中左肺下叶后基底段结节较前稍增大,评价SD;左肺上叶、右肺水平裂、左肺下叶、右肺中叶小结节,性质待定,较前增多。
仔细阅片讨论,考虑病灶局限于左肺尖及下叶后基底段两个部位,其他肺结节暂不考虑转移。
2021-06-11至06-23行肺部A段SBRT放疗(为左下肺病灶,PTV11 54Gy/6F,PTV12 45Gy/6F)。2021-07-14至2021-07-26起予肺部B段(左肺尖)SBRT放疗;48Gy/6F。
SBRT完成后建议患者继续接受PD-1抗体+TKI治疗,患者拒绝,要求定期复查。
2022-02-11复查CT:未见明显肿瘤残留。
CEA变化情况:

病例总结:

患者术前诊断直肠癌cT4aN2M1,Dixon术后考虑分期为IVA期,基因检测示MSS,TMB-L(9.6Muts/Mb),行1程XELOX方案化疗后患者拒绝继续接受辅助治疗。术后8月复查发现肺转移,予帕博丽珠单抗+呋喹替尼/瑞戈菲尼治疗6程后(期间因副反应明显停止治疗)复查肺部病灶稳定,新发右肾上腺转移灶;继续予帕博丽珠单抗治疗3程后行右肾上腺肿物切除,术后继续予PD-1治疗4程;复查提示肺部转移灶稍增大,遂行肺转移灶SBRT。放疗结束后患者拒绝继续接受PD-1治疗,定期复查,无瘤生存至今。
丁培荣教授点评:
患者初始治疗后诊断为直肠癌伴腹膜后淋巴结转移(IVA期),R0切除,基因检测提示MSS,RAS突变,按目前指南应该接受术后辅助化疗,但接受一程化疗后拒绝继续化疗。发现肺转移后仍然拒绝常规化疗。美国FDA根据Keynote-158研究结果批准了肿瘤突变负荷(TMB)>10个突变/Mb且既往治疗后疾病进展的无法切除或转移性实体瘤患者。该研究显示,高TMB组的ORR高达30.3%,高TMB非MSI-H组ORR为27.1%,而非高TMB组的ORR只有6.7%。另一方面,REGONIVO等研究显示MSS型转移性结直肠癌标准治疗失败后PD-1抗体联合抗血管生成TKI能使部分患者获益,其中尤其肺转移患者是获益的主要人群。考虑患者TMB接近10Muts/Mb且病灶均局限于肺,因此选择予PD-1抗体+TKI治疗。治疗后虽然出现右侧肾上腺转移,但肺部病灶控制尚稳定,经局部手术(肾上腺)和放疗后(肺部)获得无瘤生存,提示免疫治疗可能使MSS直肠癌中TMB相对较高的患者获益,为今后MSS直肠癌的治疗提供新的思路。
有研究显示,肾上腺是免疫耐受器官,当黑色素瘤发生肾上腺转移时,免疫治疗的应答明显低于其他转移部位。本例患者的治疗经过也印证了其他瘤种的发现。出现肾上腺转移整体评价为治疗进展,按照常规的治疗策略应该是更换方案治疗。但细致的分析发现,本例患者的转移特点是局限进展,即仅仅是免疫耐受器官出现肿瘤进展,其他转移灶控制良好,本团队认为这种局限性进展应该区别对待。积极的局部治疗可去除局限性耐药病灶,为患者继续免疫治疗提供机会。同样道理,在全身治疗有效的情况下,积极通过局部治疗毁损控制良好的转移灶(肺)是所有转移性结直肠癌应该遵循的治疗策略。
临床上存在部分患者因为客观或主管原因(高龄、伴发病、化疗反应及个人意愿等)未能接受标准化疗,可能会使疗效受到一定的影响。但患者仍有接受治疗的意愿,因此如何根据患者的生理功能情况、治疗潜在的毒性和患者意愿制定一个能被接受和执行的方案是很有挑战性的任务。本例患者是一个代表性的案例,因为自身极其抗拒化疗而使治疗面临中断和疾病持续进展的风险。但是本团队在充分理解患者的意愿和身体生理功能状态的情况下,根据分子特点及目前有限的研究数据为患者提供了备选方案,并最终取得了较理想的疗效。
本图文来自中山大学肿瘤防治中心。仅供读者参考,著作权、版权归属原创者所有。转载此文是出于传递更多正能量信息之目的,侵权删
中山大学肿瘤防治中心
丁培荣教授
广东省杰出青年医学人才(首批)
美国外科学院院士(FACS)
中国抗癌协会家族遗传性肿瘤专业委员会 副主任委员
中国临床肿瘤学会(CSCO)青年专家委员会 副主任委员
广东省抗癌协会遗传性肿瘤专业委员会 主任委员






 首页
首页

 癌症科普
癌症科普

 癌症种类
癌症种类

 药品百科
药品百科

 肿瘤医院
肿瘤医院

 名医专家
名医专家

 免费试新药
免费试新药

 健康资讯
健康资讯

 癌症新方案
癌症新方案














